
5. അലോഹ സംയുക്തങ്ങൾ
പ്രധാന ആശയങ്ങൾ
* അമോണിയ വാതകം പരീക്ഷണശാലയിൽ നിർമിക്കുന്നവിധം.
* അമോണിയയുടെ ജലത്തിലെ ലേയത്വം-ഫൗണ്ടൻ പരീക്ഷണം
* അമോണിയം ക്ലോറൈഡിന്റെ വിഘടനം
* ഏകദിശാ പ്രവർത്തനങ്ങൾ, ഉഭയദിശാപ്രവർത്തനങ്ങൾ
* രാസസംതുലനം - ഗ്രാഫ്, സവിശേഷതകൾ
* ലെ - ഷാറ്റ്ലിയർ തത്ത്വം
* സംതുലനാവസ്ഥയിൽ ഗാഢത, താപനില, മർദം, ഉൽപ്രേരകം എന്നിവയുടെ സ്വാധീനം
* സൾഫ്യൂരിക് ആസിഡ് - ഉപയോഗങ്ങൾ, വ്യാവസായിക നിർമാണം, ഭൗതിക, രാസഗുണങ്ങൾ
* സൾഫേറ്റുകളുടെ ശോധനാ പരീക്ഷണം
പ്രത്യേക ശ്രദ്ധയ്ക്ക്
1. അമോണിയയുടെ ഭൗതിക, രാസഗുണങ്ങൾ (രൂക്ഷഗന്ധം, ബേസികസ്വഭാവം, കുറഞ്ഞ സാന്ദ്രത, ജലത്തിലെ ഉയർന്ന ലേയത്വം)
2. രാസസംതുലനം തന്മാത്രാതലത്തിൽ ഗതികമാണ്. കാരണം പ്രവർത്തനം നിലച്ചുവെന്ന് തോന്നുമെങ്കിലും പുരോ-പശ്ചാത് പ്രവർത്തനങ്ങൾ ഒരേനിരക്കിൽ നടന്നുകൊണ്ടിരിക്കുന്നു.
3. മർദത്തിന് സംതുലനാവസ്ഥയിൽ സ്വാധീനമില്ലാത്ത രാസപ്രവർത്തനങ്ങൾ (അഭികാരകങ്ങളും ഉല്പന്നങ്ങളും വാതകാവസ്ഥയിൽ അല്ലാത്തപ്പോഴും, അഭികാരക-ഉല്പന്ന തന്മാത്രകളുടെ എണ്ണം തുല്യമായിരിക്കുന്പോഴും)
4. ഉഭയദിശാ പ്രവർത്തനങ്ങളിൽ ഉൽപ്രേരകങ്ങൾ പുരോ-പശ്ചാത് പ്രവർത്തനങ്ങളുടെ വേഗതയെ ഒരേ നിരക്കിൽ വർധിപ്പിക്കുന്നതിനാൽ വ്യൂഹം വേഗത്തിൽ സംതുലനാവസ്ഥ പ്രാപിക്കുന്നു.
5. നിർജലീകരണം (പദാർഥങ്ങളിൽ രാസപരമായി യോജിച്ചിരിക്കുന്ന ജലത്തെ നീക്കം ചെയ്യുന്ന പ്രവർത്തനം)
ഉദാ: പഞ്ചസാര, കോട്ടൺ തുണി, ഗ്ലൂക്കോസ്, കോപ്പർ സൾഫേറ്റ് (തുരിശ്) ക്രിസ്റ്റലുകൾ എന്നിവയിൽ സൾഫ്യൂരിക്കാസിഡിന്റെ പ്രവർത്തനം.
6. ശോഷകാരകഗുണം (ഒരു പദാർഥത്തോടൊപ്പമുള്ള ജലാംശത്തെ ആഗിരണം ചെയ്യുന്ന പ്രവർത്തനം.
ഉദാ. ക്ലോറിൻ, സൾഫർ ഡൈ ഓക്സൈഡ്, ഹൈഡ്രജൻ ക്ലോറൈഡ് എന്നിവ ഈർപ്പരഹിതമാക്കാൻ H2SO4 ഉപയോഗിക്കുന്നു.
7. മറ്റ് ആസിഡുകളുടെ നിർമാണത്തിന് H2SO4 ഉപയോഗിക്കുന്നു. ക്ലോറൈഡുകളുമായി പ്രവർത്തിച്ച് ഹൈഡ്രോ ക്ലോറിക് ആസിഡും, നൈട്രേറ്റുമായി പ്രവർത്തിച്ച് നൈട്രിക് ആസിഡും നിർമിക്കുന്നു.
8. H2SO4 ന്റെ ഓക്സീകരണ ഗുണം
ഉദാ. അലോഹമായ കാർബണിനെ CO2 ആയും ലോഹമായ കോപ്പറിനെ CuSO4 ആയും ഓക്സീകരിക്കുന്നു.
6. ഓർഗാനിക് സംയുക്തങ്ങളുടെ നാമകരണവും ഐസോമെറിസവും
പ്രധാന ആശയങ്ങൾ
* ഓർഗാനിക് സംയുക്തങ്ങളുടെ ഘടന, തന്മാത്രാസൂത്രം, കണ്ടൻസ്ഡ് ഫോർമുല
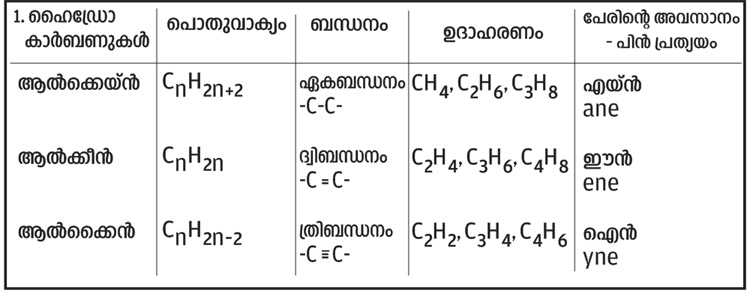
* പൂരിത ഹൈഡ്രോ കാർബണുകൾ-ആൽക്കെയ്നുകൾ
* അപൂരിത ഹൈഡ്രോ കാർബണുകൾ - ആൽക്കീൻ, ആൽക്കൈൻ
* ഹോമലോഗസ് സീരീസ്
* ശാഖകളില്ലാത്ത ആൽക്കെയ്നുകളുടെ നാമകരണം
* ശാഖകളുള്ള (ഒന്നോ, ഒന്നിലധികമോ) ഹൈഡ്രോ കാർബണുകളുടെ നാമകരണം.
* ആൽക്കീനുകളുടെയും ആൽക്കൈനുകളുടെയും നാമകരണം.
* വലയസംയുക്തങ്ങൾ -ആലിസൈക്ലിക്, ആരോമാറ്റിക്
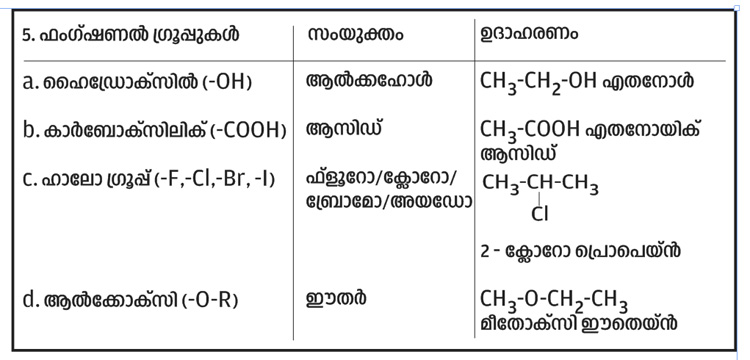
* ഫംഗ്ഷണൽ ഗ്രൂപ്പുകൾ
* ഐസോമെറിസം (ചെയിൻ, ഫങ്ഷണൽ, പൊസിഷൻ)
പ്രത്യേക ശ്രദ്ധയ്ക്ക്
2. ഹൈഡ്രോ കാർബണുകൾക്കു പേരുനല്കുന്പോൾ
a. ശാഖകളില്ലാത്ത ആൽക്കെയ്ൻ
പദമൂലം (C1 -മീത്, C2 -ഈത്, C3-പ്രൊപ്, C4 -ബ്യൂട്ട്, C5-പെന്റ്,
C6- ഹെക്സ്, C7-ഹെപ്റ്റ്, C8-ഒക്റ്റ്, C9-നൊൺ, C10-ഡെക്)+എയ്ൻ
ഉദാ.
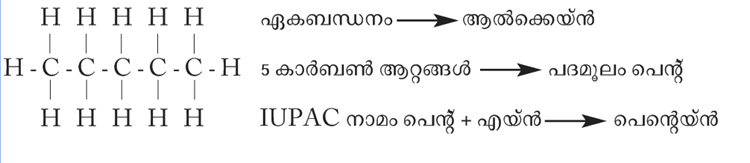
b. ശാഖകളുള്ള ആൽക്കെയ്ൻ ശാഖകളുടെ സ്ഥാനസംഖ്യ + ഹൈഫൻ + റാഡിക്കലിന്റെ പേര് + പദമൂലം
+ പിൻ പ്രത്യയം
ഉദാ.
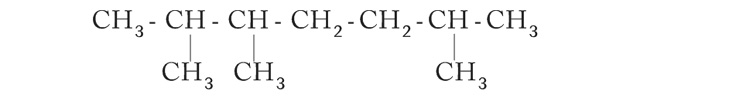
IUPAC നാമം: 2, 3, 6 - ട്രൈമീതൈൽ ഹെപ്റ്റെയ്ൻ
2, 3, 6 - ശാഖകളുടെ സ്ഥാനസംഖ്യ (കുറഞ്ഞ സ്ഥാനസംഖ്യ, ഇടത്തുനിന്ന്
വലത്തോട്ട്)
ട്രൈ - ശാഖകളുടെ എണ്ണം (3)
മീതൈൽ - റാഡിക്കലിന്റെ പേര് (CH3)
ഹെപ്റ്റ് - മുഖ്യചെയിനിലെ കാർബൺ ആറ്റങ്ങളുടെ എണ്ണം (7)
എയ്ൻ - പിൻ പ്രത്യയം (ഏകബന്ധനം, ആൽക്കെയ്ൻ)
3. സംയുക്തത്തിന്റെ പേരു തന്നാൽ ഘടനാവാക്യം എഴുതാൻ
ഉദാ. 2, 3, 3 - ട്രൈമീതൈൽ പെന്റെയ്ൻ
മുഖ്യചെയിനിലെ കാർബൺ ആറ്റങ്ങളുടെ എണ്ണം (പെന്റ്) -5
കാർബൺ ആറ്റങ്ങൾക്കിടയിലെ ബന്ധനം (എയ്ൻ) ഏകബന്ധനം
ശാഖകളുടെ സ്ഥാനം - 2, 3, 3
ശാഖകളുടെ എണ്ണം - 3 (ട്രൈ)
ശാഖകളുടെ ഘടന - CH3 (മീതൈൽ)
കാർബണിന്റെ സംയോജകത - 4
മുഖ്യ ചെയിനിലെ അഞ്ച് C ആറ്റങ്ങളും ശാഖകളും എഴുതിയതിനുശേഷം
"C' യുടെ സംയോജകത പൂർത്തീകരിക്കാൻ ആവശ്യമായ ഹൈഡ്രജൻ
നല്കിയാൽ
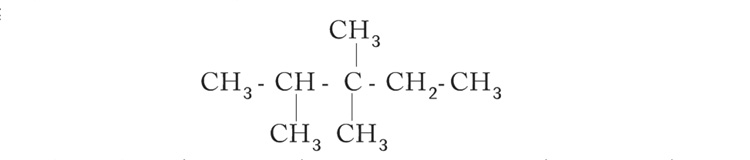
4. ആൽക്കീനുകൾക്കും (ദ്വിബന്ധനം) ആൽക്കൈനുകൾക്കും (ത്രിബന്ധനം) പേരു നല്കുന്പോൾ ദ്വിബന്ധനമോ ത്രിബന്ധനമോ വഴി ചേർന്നിരിക്കുന്ന കാർബൺ ആറ്റങ്ങൾക്ക് കുറഞ്ഞ സ്ഥാനസംഖ്യ നല്കുക. പിൻപ്രത്യയം ഈൻ/ഐൻ.
ഉദാ. CH3 - CH = CH - CH3 ബ്യൂട്ട് - 2 - ഈൻ (C4H8)
CH3 - C = C - CH3 ബ്യൂട്ട് -2 - ഐൻ (C4H6)
6. ഐസോമെറിസം - ഒരേ തന്മാത്രാവാക്യം, വ്യത്യസ്ത ഘടനാവാക്യം
a) ചെയിൻ ഐസോമെറിസം - ചെയിൻ ഘടനയിൽ വ്യത്യാസം
b) ഫംഗ്ഷണൽ ഐസോമെറിസം - ഫംഗ്ഷണൽ ഗ്രൂപ്പുകൾ വ്യത്യസ്തം
c) പൊസിഷൻ ഐസോമെറിസം - ഒരേ ഫംഗ്ഷണൽ ഗ്രൂപ്പ്, എന്നാൽ അവയുടെ സ്ഥാനം വ്യത്യസ്തം
7. ഓർഗാനിക് സംയുക്തങ്ങളുടെ രാസപ്രവർത്തനങ്ങൾ
പ്രധാന ആശയങ്ങൾ
* ആദേശ രാസപ്രവർത്തനങ്ങൾ
* അഡിഷൻ രാസപ്രവർത്തനങ്ങൾ
* പോളിമെറൈസേഷൻ
* ഹൈഡ്രോകാർബണുകളുടെ ജ്വലനം
* താപീയ വിഘടനം
* ആൽക്കഹോളുകൾ
* മെതനോളിന്റെയും എതനോളിന്റെയും നിർമാണം, ഉപയോഗങ്ങൾ
* കാർബോക്സിലിക് ആസിഡുകൾ
* എതനോയിക് ആസിഡിന്റെ നിർമാണം
* എസ്റ്ററുകൾ - എസ്റ്ററിഫിക്കേഷൻ
* സോപ്പ്-നിർമാണം, ശുചീകരണ പ്രവർത്തനം
* ഡിറ്റർജന്റുകൾ - മേന്മകൾ, പരിമിതി (പാരിസ്ഥിതിക പ്രശ്നങ്ങൾ)
പ്രത്യേകം ശ്രദ്ധിക്കാം
1. ആദേശ രാസപ്രവർത്തനങ്ങൾ പൂരിതസംയുക്തങ്ങളുടെയും (ആൽക്കെയ്നുകൾ), അഡിഷൻ പ്രവർത്തനങ്ങൾ അപൂരിത സംയുക്തങ്ങളുടെയും (ആൽക്കീൻ, ആൽക്കൈൻ) സവിശേഷ പ്രവർത്തനങ്ങളാണ്.
ആദേശപ്രവർത്തനങ്ങളിൽ അഭികാരകത്തിലെ ഒരു ആറ്റത്തെ മാറ്റി അതിന്റെ സ്ഥാനത്ത് മറ്റൊരു ആറ്റമോ ആറ്റം ഗ്രൂപ്പോ വരും. അഡിഷൻ പ്രവർത്തനഫലമായി അപൂരിത സംയുക്തങ്ങൾ പൂരിതമായി മാറും.
2. പോളിമെറൈസേഷനിൽ അനേകം ലഘുതന്മാത്രകൾ (മോണോമെറുകൾ) കൂട്ടിച്ചേർത്ത് സങ്കീർണതന്മാത്രകളായി (പോളിമെറുകൾ) മാറുന്നു.
3. ഹൈഡ്രോ കാർബണുകളുടെ ജ്വലനഫലമായി (ഓക്സിജനുമായുള്ള ചേരൽ) കാർബൺ ഡൈ ഓക്സൈഡും ജലവും ഉണ്ടാകുന്നു. താപമോചക പ്രവർത്തനമായതിനാൽ ഇന്ധനമായി ഉപയോഗിക്കപ്പെടുന്നു.
4. താപീയ വിഘടനത്തിൽ തന്മാത്രാഭാരം കൂടുതലുള്ള ഒരു സംയുക്തം (അഭികാരകം) ചൂടാകുന്പോൾ വിഘടിച്ച് ഒന്നിലധികം ലഘുഹൈഡ്രോകാർബണുകൾ (ഉല്പന്നം) ആയി മാറുന്നു.
5. വുഡ് സ്പിരിറ്റ് - മെതനോൾ
ഗ്രേയ്പ് സ്പിരിറ്റ് - എതനോൾ
വാഷ് - 8-10% എതനോൾ
റെക്റ്റിഫൈഡ് സ്പിരിറ്റ് - 95.6% വീര്യമുള്ള എതനോൾ
ഡിനേച്ചേർഡ് സ്പിരിറ്റ് - വിഷം ചേർത്ത എതനോൾ (വിഷമദ്യം)
മെതിലേറ്റഡ് സ്പിരിറ്റ് - മെതനോൾ (വിഷം) ചേർത്ത എതനോൾ(വിഷമദ്യം)
അബ്സൊല്യൂട്ട് ആൽക്കഹോൾ - 99% ശുദ്ധമായ എതനോൾ
പവർ ആൽക്കഹോൾ (ഇന്ധനം) - അബ്സൊല്യൂട്ട് ആൽക്കഹോൾ
+ പെട്രോൾ
6. ആൽക്കഹോൾ + ഓർഗാനിക് ആസിഡ് എസ്റ്റർ + ജലം
(എസ്റ്ററിഫിക്കേഷൻ) - ഫങ്ഷണൽ ഗ്രൂപ്പ് -COO-
7. പാമിറ്റിക്/സ്റ്റിയറിക്/ഓലിയിക് ആസിഡ് + ഗ്ലിസറോൾ എണ്ണ/കൊഴുപ്പ്
എണ്ണ/കൊഴുപ്പ് + ആൽക്കലി സോപ്പ്
സോപ്പ് തന്മാത്രയിലെ പോളാർ അഗ്രം ജലത്തിലും നോൺ പോളാർ അഗ്രം എണ്ണകളിലും ലയിക്കുന്നു. സോപ്പ്, ജലത്തിന്റെ പ്രതലബലം കുറയ്ക്കുകയും തുണി നന്നായി നനയുകയും ചെയ്യുന്നു. ഇങ്ങനെ സോപ്പ് അഴുക്കിനെ നീക്കം ചെയ്യുന്നു.
8. ഡിറ്റർജന്റുകൾ സൾഫോണിക് ആസിഡിന്റെ ലവണങ്ങളാണ്. കഠിന ജലത്തിലും പതയുന്നു. അസിഡിക് ലായനികളിലും ഉപയോഗിക്കാം. ഡിറ്റർജന്റുകൾ ആൽഗകളുടെ വളർച്ച ത്വരിതപ്പെടുത്തുകയും ഓക്സിജന്റെ അളവ് കുറയ്ക്കുകയും ജലജീവികളുടെ നിലനില്പ് അപകടത്തിലാക്കുകയും ചെയ്യുന്നു.
ബാബു ടി. ജോൺ
അസ്ത്രാ അക്കാഡമി, കാഞ്ഞിരപ്പള്ളി.
പ്രധാന ആശയങ്ങൾ
* അമോണിയ വാതകം പരീക്ഷണശാലയിൽ നിർമിക്കുന്നവിധം.
* അമോണിയയുടെ ജലത്തിലെ ലേയത്വം-ഫൗണ്ടൻ പരീക്ഷണം
* അമോണിയം ക്ലോറൈഡിന്റെ വിഘടനം
* ഏകദിശാ പ്രവർത്തനങ്ങൾ, ഉഭയദിശാപ്രവർത്തനങ്ങൾ
* രാസസംതുലനം - ഗ്രാഫ്, സവിശേഷതകൾ
* ലെ - ഷാറ്റ്ലിയർ തത്ത്വം
* സംതുലനാവസ്ഥയിൽ ഗാഢത, താപനില, മർദം, ഉൽപ്രേരകം എന്നിവയുടെ സ്വാധീനം
* സൾഫ്യൂരിക് ആസിഡ് - ഉപയോഗങ്ങൾ, വ്യാവസായിക നിർമാണം, ഭൗതിക, രാസഗുണങ്ങൾ
* സൾഫേറ്റുകളുടെ ശോധനാ പരീക്ഷണം
പ്രത്യേക ശ്രദ്ധയ്ക്ക്
1. അമോണിയയുടെ ഭൗതിക, രാസഗുണങ്ങൾ (രൂക്ഷഗന്ധം, ബേസികസ്വഭാവം, കുറഞ്ഞ സാന്ദ്രത, ജലത്തിലെ ഉയർന്ന ലേയത്വം)
2. രാസസംതുലനം തന്മാത്രാതലത്തിൽ ഗതികമാണ്. കാരണം പ്രവർത്തനം നിലച്ചുവെന്ന് തോന്നുമെങ്കിലും പുരോ-പശ്ചാത് പ്രവർത്തനങ്ങൾ ഒരേനിരക്കിൽ നടന്നുകൊണ്ടിരിക്കുന്നു.
3. മർദത്തിന് സംതുലനാവസ്ഥയിൽ സ്വാധീനമില്ലാത്ത രാസപ്രവർത്തനങ്ങൾ (അഭികാരകങ്ങളും ഉല്പന്നങ്ങളും വാതകാവസ്ഥയിൽ അല്ലാത്തപ്പോഴും, അഭികാരക-ഉല്പന്ന തന്മാത്രകളുടെ എണ്ണം തുല്യമായിരിക്കുന്പോഴും)
4. ഉഭയദിശാ പ്രവർത്തനങ്ങളിൽ ഉൽപ്രേരകങ്ങൾ പുരോ-പശ്ചാത് പ്രവർത്തനങ്ങളുടെ വേഗതയെ ഒരേ നിരക്കിൽ വർധിപ്പിക്കുന്നതിനാൽ വ്യൂഹം വേഗത്തിൽ സംതുലനാവസ്ഥ പ്രാപിക്കുന്നു.
5. നിർജലീകരണം (പദാർഥങ്ങളിൽ രാസപരമായി യോജിച്ചിരിക്കുന്ന ജലത്തെ നീക്കം ചെയ്യുന്ന പ്രവർത്തനം)
ഉദാ: പഞ്ചസാര, കോട്ടൺ തുണി, ഗ്ലൂക്കോസ്, കോപ്പർ സൾഫേറ്റ് (തുരിശ്) ക്രിസ്റ്റലുകൾ എന്നിവയിൽ സൾഫ്യൂരിക്കാസിഡിന്റെ പ്രവർത്തനം.
6. ശോഷകാരകഗുണം (ഒരു പദാർഥത്തോടൊപ്പമുള്ള ജലാംശത്തെ ആഗിരണം ചെയ്യുന്ന പ്രവർത്തനം.
ഉദാ. ക്ലോറിൻ, സൾഫർ ഡൈ ഓക്സൈഡ്, ഹൈഡ്രജൻ ക്ലോറൈഡ് എന്നിവ ഈർപ്പരഹിതമാക്കാൻ H2SO4 ഉപയോഗിക്കുന്നു.
7. മറ്റ് ആസിഡുകളുടെ നിർമാണത്തിന് H2SO4 ഉപയോഗിക്കുന്നു. ക്ലോറൈഡുകളുമായി പ്രവർത്തിച്ച് ഹൈഡ്രോ ക്ലോറിക് ആസിഡും, നൈട്രേറ്റുമായി പ്രവർത്തിച്ച് നൈട്രിക് ആസിഡും നിർമിക്കുന്നു.
8. H2SO4 ന്റെ ഓക്സീകരണ ഗുണം
ഉദാ. അലോഹമായ കാർബണിനെ CO2 ആയും ലോഹമായ കോപ്പറിനെ CuSO4 ആയും ഓക്സീകരിക്കുന്നു.
6. ഓർഗാനിക് സംയുക്തങ്ങളുടെ നാമകരണവും ഐസോമെറിസവും
പ്രധാന ആശയങ്ങൾ
* ഓർഗാനിക് സംയുക്തങ്ങളുടെ ഘടന, തന്മാത്രാസൂത്രം, കണ്ടൻസ്ഡ് ഫോർമുല
* പൂരിത ഹൈഡ്രോ കാർബണുകൾ-ആൽക്കെയ്നുകൾ
* അപൂരിത ഹൈഡ്രോ കാർബണുകൾ - ആൽക്കീൻ, ആൽക്കൈൻ
* ഹോമലോഗസ് സീരീസ്
* ശാഖകളില്ലാത്ത ആൽക്കെയ്നുകളുടെ നാമകരണം
* ശാഖകളുള്ള (ഒന്നോ, ഒന്നിലധികമോ) ഹൈഡ്രോ കാർബണുകളുടെ നാമകരണം.
* ആൽക്കീനുകളുടെയും ആൽക്കൈനുകളുടെയും നാമകരണം.
* വലയസംയുക്തങ്ങൾ -ആലിസൈക്ലിക്, ആരോമാറ്റിക്
* ഫംഗ്ഷണൽ ഗ്രൂപ്പുകൾ
* ഐസോമെറിസം (ചെയിൻ, ഫങ്ഷണൽ, പൊസിഷൻ)

പ്രത്യേക ശ്രദ്ധയ്ക്ക്
2. ഹൈഡ്രോ കാർബണുകൾക്കു പേരുനല്കുന്പോൾ
a. ശാഖകളില്ലാത്ത ആൽക്കെയ്ൻ
പദമൂലം (C1 -മീത്, C2 -ഈത്, C3-പ്രൊപ്, C4 -ബ്യൂട്ട്, C5-പെന്റ്,
C6- ഹെക്സ്, C7-ഹെപ്റ്റ്, C8-ഒക്റ്റ്, C9-നൊൺ, C10-ഡെക്)+എയ്ൻ
ഉദാ.

b. ശാഖകളുള്ള ആൽക്കെയ്ൻ ശാഖകളുടെ സ്ഥാനസംഖ്യ + ഹൈഫൻ + റാഡിക്കലിന്റെ പേര് + പദമൂലം
+ പിൻ പ്രത്യയം
ഉദാ.
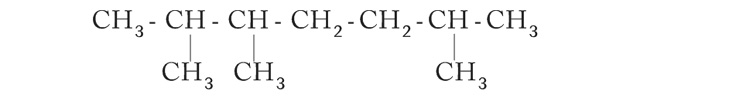
IUPAC നാമം: 2, 3, 6 - ട്രൈമീതൈൽ ഹെപ്റ്റെയ്ൻ
2, 3, 6 - ശാഖകളുടെ സ്ഥാനസംഖ്യ (കുറഞ്ഞ സ്ഥാനസംഖ്യ, ഇടത്തുനിന്ന്
വലത്തോട്ട്)
ട്രൈ - ശാഖകളുടെ എണ്ണം (3)
മീതൈൽ - റാഡിക്കലിന്റെ പേര് (CH3)
ഹെപ്റ്റ് - മുഖ്യചെയിനിലെ കാർബൺ ആറ്റങ്ങളുടെ എണ്ണം (7)
എയ്ൻ - പിൻ പ്രത്യയം (ഏകബന്ധനം, ആൽക്കെയ്ൻ)
3. സംയുക്തത്തിന്റെ പേരു തന്നാൽ ഘടനാവാക്യം എഴുതാൻ
ഉദാ. 2, 3, 3 - ട്രൈമീതൈൽ പെന്റെയ്ൻ
മുഖ്യചെയിനിലെ കാർബൺ ആറ്റങ്ങളുടെ എണ്ണം (പെന്റ്) -5
കാർബൺ ആറ്റങ്ങൾക്കിടയിലെ ബന്ധനം (എയ്ൻ) ഏകബന്ധനം
ശാഖകളുടെ സ്ഥാനം - 2, 3, 3
ശാഖകളുടെ എണ്ണം - 3 (ട്രൈ)
ശാഖകളുടെ ഘടന - CH3 (മീതൈൽ)
കാർബണിന്റെ സംയോജകത - 4
മുഖ്യ ചെയിനിലെ അഞ്ച് C ആറ്റങ്ങളും ശാഖകളും എഴുതിയതിനുശേഷം
"C' യുടെ സംയോജകത പൂർത്തീകരിക്കാൻ ആവശ്യമായ ഹൈഡ്രജൻ
നല്കിയാൽ

4. ആൽക്കീനുകൾക്കും (ദ്വിബന്ധനം) ആൽക്കൈനുകൾക്കും (ത്രിബന്ധനം) പേരു നല്കുന്പോൾ ദ്വിബന്ധനമോ ത്രിബന്ധനമോ വഴി ചേർന്നിരിക്കുന്ന കാർബൺ ആറ്റങ്ങൾക്ക് കുറഞ്ഞ സ്ഥാനസംഖ്യ നല്കുക. പിൻപ്രത്യയം ഈൻ/ഐൻ.
ഉദാ. CH3 - CH = CH - CH3 ബ്യൂട്ട് - 2 - ഈൻ (C4H8)
CH3 - C = C - CH3 ബ്യൂട്ട് -2 - ഐൻ (C4H6)

6. ഐസോമെറിസം - ഒരേ തന്മാത്രാവാക്യം, വ്യത്യസ്ത ഘടനാവാക്യം
a) ചെയിൻ ഐസോമെറിസം - ചെയിൻ ഘടനയിൽ വ്യത്യാസം
b) ഫംഗ്ഷണൽ ഐസോമെറിസം - ഫംഗ്ഷണൽ ഗ്രൂപ്പുകൾ വ്യത്യസ്തം
c) പൊസിഷൻ ഐസോമെറിസം - ഒരേ ഫംഗ്ഷണൽ ഗ്രൂപ്പ്, എന്നാൽ അവയുടെ സ്ഥാനം വ്യത്യസ്തം
7. ഓർഗാനിക് സംയുക്തങ്ങളുടെ രാസപ്രവർത്തനങ്ങൾ
പ്രധാന ആശയങ്ങൾ
* ആദേശ രാസപ്രവർത്തനങ്ങൾ
* അഡിഷൻ രാസപ്രവർത്തനങ്ങൾ
* പോളിമെറൈസേഷൻ
* ഹൈഡ്രോകാർബണുകളുടെ ജ്വലനം
* താപീയ വിഘടനം
* ആൽക്കഹോളുകൾ
* മെതനോളിന്റെയും എതനോളിന്റെയും നിർമാണം, ഉപയോഗങ്ങൾ
* കാർബോക്സിലിക് ആസിഡുകൾ
* എതനോയിക് ആസിഡിന്റെ നിർമാണം
* എസ്റ്ററുകൾ - എസ്റ്ററിഫിക്കേഷൻ
* സോപ്പ്-നിർമാണം, ശുചീകരണ പ്രവർത്തനം
* ഡിറ്റർജന്റുകൾ - മേന്മകൾ, പരിമിതി (പാരിസ്ഥിതിക പ്രശ്നങ്ങൾ)
പ്രത്യേകം ശ്രദ്ധിക്കാം
1. ആദേശ രാസപ്രവർത്തനങ്ങൾ പൂരിതസംയുക്തങ്ങളുടെയും (ആൽക്കെയ്നുകൾ), അഡിഷൻ പ്രവർത്തനങ്ങൾ അപൂരിത സംയുക്തങ്ങളുടെയും (ആൽക്കീൻ, ആൽക്കൈൻ) സവിശേഷ പ്രവർത്തനങ്ങളാണ്.
ആദേശപ്രവർത്തനങ്ങളിൽ അഭികാരകത്തിലെ ഒരു ആറ്റത്തെ മാറ്റി അതിന്റെ സ്ഥാനത്ത് മറ്റൊരു ആറ്റമോ ആറ്റം ഗ്രൂപ്പോ വരും. അഡിഷൻ പ്രവർത്തനഫലമായി അപൂരിത സംയുക്തങ്ങൾ പൂരിതമായി മാറും.
2. പോളിമെറൈസേഷനിൽ അനേകം ലഘുതന്മാത്രകൾ (മോണോമെറുകൾ) കൂട്ടിച്ചേർത്ത് സങ്കീർണതന്മാത്രകളായി (പോളിമെറുകൾ) മാറുന്നു.
3. ഹൈഡ്രോ കാർബണുകളുടെ ജ്വലനഫലമായി (ഓക്സിജനുമായുള്ള ചേരൽ) കാർബൺ ഡൈ ഓക്സൈഡും ജലവും ഉണ്ടാകുന്നു. താപമോചക പ്രവർത്തനമായതിനാൽ ഇന്ധനമായി ഉപയോഗിക്കപ്പെടുന്നു.
4. താപീയ വിഘടനത്തിൽ തന്മാത്രാഭാരം കൂടുതലുള്ള ഒരു സംയുക്തം (അഭികാരകം) ചൂടാകുന്പോൾ വിഘടിച്ച് ഒന്നിലധികം ലഘുഹൈഡ്രോകാർബണുകൾ (ഉല്പന്നം) ആയി മാറുന്നു.
5. വുഡ് സ്പിരിറ്റ് - മെതനോൾ
ഗ്രേയ്പ് സ്പിരിറ്റ് - എതനോൾ
വാഷ് - 8-10% എതനോൾ
റെക്റ്റിഫൈഡ് സ്പിരിറ്റ് - 95.6% വീര്യമുള്ള എതനോൾ
ഡിനേച്ചേർഡ് സ്പിരിറ്റ് - വിഷം ചേർത്ത എതനോൾ (വിഷമദ്യം)
മെതിലേറ്റഡ് സ്പിരിറ്റ് - മെതനോൾ (വിഷം) ചേർത്ത എതനോൾ(വിഷമദ്യം)
അബ്സൊല്യൂട്ട് ആൽക്കഹോൾ - 99% ശുദ്ധമായ എതനോൾ
പവർ ആൽക്കഹോൾ (ഇന്ധനം) - അബ്സൊല്യൂട്ട് ആൽക്കഹോൾ
+ പെട്രോൾ
6. ആൽക്കഹോൾ + ഓർഗാനിക് ആസിഡ് എസ്റ്റർ + ജലം
(എസ്റ്ററിഫിക്കേഷൻ) - ഫങ്ഷണൽ ഗ്രൂപ്പ് -COO-
7. പാമിറ്റിക്/സ്റ്റിയറിക്/ഓലിയിക് ആസിഡ് + ഗ്ലിസറോൾ എണ്ണ/കൊഴുപ്പ്
എണ്ണ/കൊഴുപ്പ് + ആൽക്കലി സോപ്പ്
സോപ്പ് തന്മാത്രയിലെ പോളാർ അഗ്രം ജലത്തിലും നോൺ പോളാർ അഗ്രം എണ്ണകളിലും ലയിക്കുന്നു. സോപ്പ്, ജലത്തിന്റെ പ്രതലബലം കുറയ്ക്കുകയും തുണി നന്നായി നനയുകയും ചെയ്യുന്നു. ഇങ്ങനെ സോപ്പ് അഴുക്കിനെ നീക്കം ചെയ്യുന്നു.
8. ഡിറ്റർജന്റുകൾ സൾഫോണിക് ആസിഡിന്റെ ലവണങ്ങളാണ്. കഠിന ജലത്തിലും പതയുന്നു. അസിഡിക് ലായനികളിലും ഉപയോഗിക്കാം. ഡിറ്റർജന്റുകൾ ആൽഗകളുടെ വളർച്ച ത്വരിതപ്പെടുത്തുകയും ഓക്സിജന്റെ അളവ് കുറയ്ക്കുകയും ജലജീവികളുടെ നിലനില്പ് അപകടത്തിലാക്കുകയും ചെയ്യുന്നു.
ബാബു ടി. ജോൺ
അസ്ത്രാ അക്കാഡമി, കാഞ്ഞിരപ്പള്ളി.






